純化水微生物限度檢查流程
公司簡(jiǎn)介
健明迪檢測(cè)提供的純化水微生物限度檢查流程,純化水是一種用于產(chǎn)品生產(chǎn)的原輔料及清潔用水,深刻影響著產(chǎn)品的質(zhì)量問題,純化水微生物限度檢查是確保純化水質(zhì)量問題的重要環(huán)節(jié)之一,應(yīng)按照《中國(guó)藥典》2020年二版純化水微生物限度檢查的要求,進(jìn)行檢查,具體流程如下。
純化水微生物限度檢查:第四步
偏差處理情況:
驗(yàn)證的數(shù)據(jù)產(chǎn)生的任何偏差,應(yīng)及時(shí)進(jìn)行偏差調(diào)查,按照《偏差管理規(guī)程》進(jìn)行處理并如實(shí)記錄,給出合理的偏差處理措施,并上報(bào)驗(yàn)證領(lǐng)導(dǎo)小組,記錄備案,并且根據(jù)處理措施進(jìn)行相應(yīng)的處理,并對(duì)處理的過程、結(jié)果進(jìn)行記錄與跟蹤。
更多純化水檢測(cè)項(xiàng)目有哪些的問題可咨詢健明迪檢測(cè)。
純化水微生物限度檢查:第三步
試驗(yàn)結(jié)果分析:
1)計(jì)數(shù)方法適用性試驗(yàn)進(jìn)行3次獨(dú)立平行試驗(yàn)(分別使用不同取樣點(diǎn)的純化水),并分別計(jì)算各試驗(yàn)菌每次回收試驗(yàn)的比值,應(yīng)在50%~200%范圍內(nèi)。
2)試驗(yàn)組菌數(shù)回收率(%)=試驗(yàn)組的平均菌數(shù)-供試品對(duì)照組的平均菌數(shù)/菌液對(duì)照組的平均菌數(shù)×100%
3)稀釋劑對(duì)照組回收率(%)=稀釋劑對(duì)照組的平均菌數(shù)/菌液對(duì)照組的平均菌數(shù)×100%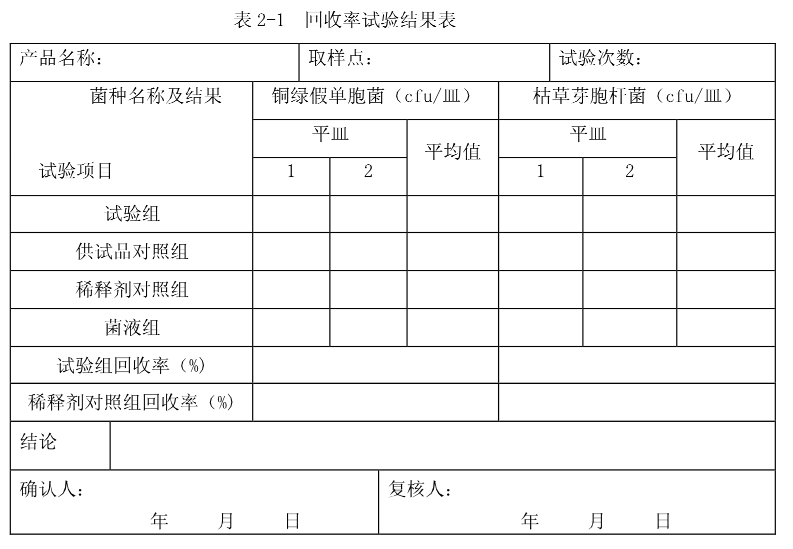 純化水微生物限度檢查:第二步
純化水微生物限度檢查:第二步
供試液的制備:
供試品:純化水
沖洗液:pH7.0無菌氯化鈉-蛋白胨緩沖液
1)試驗(yàn)組:吸取1ml供試液注入濾杯中,用pH7.0無菌氯化鈉-蛋白胨緩沖液100ml進(jìn)行過濾沖洗,分別在沖洗液中加入上述2種菌液各1ml過濾,濾干后,將薄膜用鑷子夾到已凝固的R2A瓊脂培養(yǎng)基上,平行制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定所加入的試驗(yàn)菌數(shù)。
2)供試品對(duì)照組:取供試液1ml,以稀釋液代替菌液同試驗(yàn)組操作。每個(gè)樣品各制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定供試品的菌數(shù)。
3)菌液對(duì)照組:取不含中和劑及滅活劑的相應(yīng)稀釋液替代供試液,按試驗(yàn)組操作加入試驗(yàn)菌液平行制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定其菌數(shù)。
4)稀釋劑對(duì)照組:取100ml pH7.0無菌氯化鈉-蛋白胨緩沖液注入濾杯,加入上述2種菌液各1ml進(jìn)行過濾,濾干后,將薄膜用鑷子夾到已凝固的R2A瓊脂培養(yǎng)基上。平行制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定其菌數(shù)。
純化水微生物限度檢查:第一步
菌液的制備:
取銅綠假單胞菌、枯草芽孢桿菌工作用菌種挑取少量培養(yǎng)物接種至10ml 胰酪大豆胨液體培養(yǎng)基中,30~35℃培養(yǎng)18~24小時(shí)。取該新鮮培養(yǎng)液1ml加入至0.9%無菌氯化鈉溶液中,10倍梯度稀釋至10-5~10-8,制成每1ml含菌數(shù)不大于100cfu的菌懸液。
純化水是一種用于產(chǎn)品生產(chǎn)的原輔料及清潔用水,深刻影響著產(chǎn)品的質(zhì)量問題,純化水微生物限度檢查是確保純化水質(zhì)量問題的重要環(huán)節(jié)之一,應(yīng)按照《中國(guó)藥典》2020年二版純化水微生物限度檢查的要求,進(jìn)行檢查,具體流程如下。
偏差處理情況:
驗(yàn)證的數(shù)據(jù)產(chǎn)生的任何偏差,應(yīng)及時(shí)進(jìn)行偏差調(diào)查,按照《偏差管理規(guī)程》進(jìn)行處理并如實(shí)記錄,給出合理的偏差處理措施,并上報(bào)驗(yàn)證領(lǐng)導(dǎo)小組,記錄備案,并且根據(jù)處理措施進(jìn)行相應(yīng)的處理,并對(duì)處理的過程、結(jié)果進(jìn)行記錄與跟蹤。
更多純化水檢測(cè)項(xiàng)目有哪些的問題可咨詢健明迪檢測(cè)。
純化水微生物限度檢查:第三步
試驗(yàn)結(jié)果分析:
1)計(jì)數(shù)方法適用性試驗(yàn)進(jìn)行3次獨(dú)立平行試驗(yàn)(分別使用不同取樣點(diǎn)的純化水),并分別計(jì)算各試驗(yàn)菌每次回收試驗(yàn)的比值,應(yīng)在50%~200%范圍內(nèi)。
2)試驗(yàn)組菌數(shù)回收率(%)=試驗(yàn)組的平均菌數(shù)-供試品對(duì)照組的平均菌數(shù)/菌液對(duì)照組的平均菌數(shù)×100%
3)稀釋劑對(duì)照組回收率(%)=稀釋劑對(duì)照組的平均菌數(shù)/菌液對(duì)照組的平均菌數(shù)×100%
 純化水微生物限度檢查:第二步
純化水微生物限度檢查:第二步供試液的制備:
供試品:純化水
沖洗液:pH7.0無菌氯化鈉-蛋白胨緩沖液
1)試驗(yàn)組:吸取1ml供試液注入濾杯中,用pH7.0無菌氯化鈉-蛋白胨緩沖液100ml進(jìn)行過濾沖洗,分別在沖洗液中加入上述2種菌液各1ml過濾,濾干后,將薄膜用鑷子夾到已凝固的R2A瓊脂培養(yǎng)基上,平行制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定所加入的試驗(yàn)菌數(shù)。
2)供試品對(duì)照組:取供試液1ml,以稀釋液代替菌液同試驗(yàn)組操作。每個(gè)樣品各制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定供試品的菌數(shù)。
3)菌液對(duì)照組:取不含中和劑及滅活劑的相應(yīng)稀釋液替代供試液,按試驗(yàn)組操作加入試驗(yàn)菌液平行制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定其菌數(shù)。
4)稀釋劑對(duì)照組:取100ml pH7.0無菌氯化鈉-蛋白胨緩沖液注入濾杯,加入上述2種菌液各1ml進(jìn)行過濾,濾干后,將薄膜用鑷子夾到已凝固的R2A瓊脂培養(yǎng)基上。平行制備2個(gè)平皿。在30~35℃培養(yǎng)5天,觀察結(jié)果,測(cè)定其菌數(shù)。
純化水微生物限度檢查:第一步
菌液的制備:
取銅綠假單胞菌、枯草芽孢桿菌工作用菌種挑取少量培養(yǎng)物接種至10ml 胰酪大豆胨液體培養(yǎng)基中,30~35℃培養(yǎng)18~24小時(shí)。取該新鮮培養(yǎng)液1ml加入至0.9%無菌氯化鈉溶液中,10倍梯度稀釋至10-5~10-8,制成每1ml含菌數(shù)不大于100cfu的菌懸液。
純化水是一種用于產(chǎn)品生產(chǎn)的原輔料及清潔用水,深刻影響著產(chǎn)品的質(zhì)量問題,純化水微生物限度檢查是確保純化水質(zhì)量問題的重要環(huán)節(jié)之一,應(yīng)按照《中國(guó)藥典》2020年二版純化水微生物限度檢查的要求,進(jìn)行檢查,具體流程如下。













